菱镁矿制备纳米镁铝水滑石的研究
- 发布人:管理员
- 发布时间:2015-10-28
- 浏览量:4179
张悦, 张连红, 赵驰鹏
辽宁石油化工大学 石油化工学院, 辽宁 抚顺
【摘要】以天然菱镁矿为原料,采用尿素法制备纳米Mg-Al水滑石。考察了煅烧时间和温度对菱镁矿分解率的影响。结果表明,最佳条件为700℃下煅烧0.5h。另外考察了尿素用量对水滑石形貌、尺寸、结晶度的影响,还有不同n(Mg):n( Al) 对水滑石纯度的影响。用 XRD、SEM 对产物进行分析。XRD分析结果表明, 当溶液中n(尿素):n(NO3-)=3:1时,合成的水滑石样品具有较高的结晶度; n( Mg): n( Al) = 2:1 时,合成的水滑石纯度可达到 100%;随着尿素用量的增多,合成样品的粒径逐渐增大。SEM分析结果表明,用菱镁矿合成的样品层比用硝酸镁试剂合成的样品层厚很多。
我国是世界上菱镁矿资源最为丰富的国家, 主要分布在辽宁、 山东等地, 其中以辽宁的菱镁矿储量最为丰富,占全国的 85.6%,以其质量高和规模大而闻名于世[1- 3] 。但是因为大部分矿山采用采富弃贫的传统方式,导致大量粉矿被废弃, 并且占地堆放。辽宁海城就堆存了几百万吨,这不仅严重污染了当地环境,而且影响了菱镁矿资源的高效利用[4- 5] 。因此,提高菱镁矿的粉矿利用率,开发高附加值产品,是当前我国镁质资源利用的重要发展方向。
水滑石类化合物为阴离子层状化合物, 层间具有可交换阴离子, 层板由两种不同价态的金属氢氧化物组成。因此,又称为层状双金属氢氧化物( LDHs) 。典型的水滑石类化合物 Mg6Al2(OH)16-CO3·4H2O是天然存在的层状粘土矿物之一, 其结构类似于水镁石 Mg( OH)2 的正八面体结构,于1842 年在瑞典被发现[6- 8 ]。因为水滑石独特的结构特性、 制备容易、 组成多变且可控、 本身无毒无害, 使其在催化、 吸附、 医药、 材料合成等方面展示了广阔的应用前景, 已经引起广泛关注[9- 12] 。本研究就利用粉矿率低的菱镁矿来制备 Mg- Al 水滑石以促进镁质资源的高效综合利用 [13- 15 ] 。
1 实验部分
1.1 材料与仪器
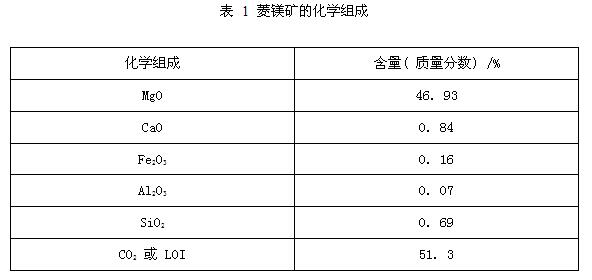
天然菱镁矿,辽宁海城,主要成分是 MgCO3, 其化学组成见表1。硝酸( HNO3 ) 、 硝酸铝[Al( NO3 )3·9H 2 O] 、硝酸镁[Mg( NO3 )2·6H2O] 、尿素(Urea)均为分析纯;蒸馏水等。JJ- 1 精密增力电动搅拌器; W- O恒温油水浴锅;SXL- 1208 马弗炉; JA5003N- 分析天平;SHB-ⅢA 循环水式多用真空泵;DZF 真空干燥箱; HKG 热重分析仪。
1.2 菱镁矿制备氧化镁
首先用热重分析仪对菱镁矿作 TG 分析, 称取菱镁矿 20.00 mg, 在N 2氛围,气流速度 50 mL/min条件下,以 10℃ /min 的升温速率将样品从20 ℃加热到850 ℃;然后根据曲线所绘考察不同温度、不同时间下对菱镁矿进行煅烧,冷却后称取煅烧产物氧化镁的质量,计算分解率。
试验中利用如下公式计算菱镁矿的分解率:
其中, 和 分别表示煅烧前后菱镁矿的质量, η表示菱镁矿的分解率。η的值越大, 表示菱镁矿煅烧得越完全。
1.3 纳米水滑石的制备
首先利用煅烧所获得的氧化镁为原料, 与一定浓度的硝酸反应,制得硝酸镁溶液;然后按n( Mg):n( Al) = 2~4的比例向溶液中加入硝酸铝,再按 n(尿素): n( NO3-) = 1~4的比例加入尿素。在装有冷凝水、温度计及搅拌装置的圆底烧瓶中反应。将溶液升温至 90 ℃,保持动态晶化 11 h,再在 95 ℃下静态晶化 18 h;然后抽滤, 用去离子水洗涤2~3 次, 将所得样品于90 ℃下干燥18 h, 即得纳米水滑石样品。
1.4 样品表征
使用日本Rigaku 公司的 D/MAX-1A 型 X 射线衍射仪( XRD) 对所制得的样品进行物相分析,CuK 靶,Ni 滤波;采用日本 HITACHI 公司生产的SU8010 型扫描电镜( SEM) 观察样品的形貌,15 kV,喷金。
2 结果与讨论
2.1 煅烧条件对菱镁矿分解率的影响
菱镁矿的 TG 曲线见图 1。

由图 1 可知,其主要的热分解区间在 400 ~800℃。TG曲线在 400℃时出现下降趋势,这说明菱镁矿400 ℃开始分解,放出 CO2 。之后,TG 曲线开始出现急剧下降,当温度到达650 ℃时趋于平稳,说明菱镁矿基本分解完全。
根据 TG 曲线所绘将菱镁矿在 600,650,700,750 ℃温度下煅烧不同时间,得出煅烧时间与菱镁矿分解率的关系,见图 2。
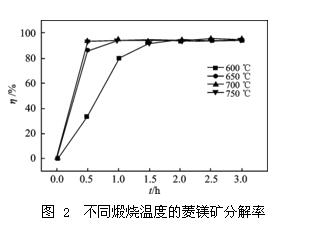
由图2可知,当煅烧温度为 600 ℃时,1.5h 可以分解完全; 温度为650 ℃时, 1 h 分解完全; 而温度达到700,750 ℃时, 0.5 h 就可以完全分解。菱镁矿分解率最高可达到 96%。这说明随着煅烧温度的升高,菱镁矿完全分解所需的时间越短。综合考虑,制备氧化镁的最佳工艺条件为700 ℃下煅烧0.5 h。
2.2 XRD 表征
对 n(Mg):n(Al) =2∶1,n(尿素):n(NO3-) =1~4 的样品水滑石作 XRD 分析,见图3。由图3可知,n(尿素):n( NO3-) =1:1时,就可以制得Mg- Al水滑石; n(尿素):n( NO3-)增加到3:1时,可以明显看出样品的结晶度越来越高;而当尿素量继续增加,对水滑石的结晶度影响不大。采用谢乐公式,计算 n(Mg): n(Al) =2:1、尿素用量不同时样品的平均粒径,得到表2。由表 2 可知,随着溶液中尿素量的增多,样品的粒径逐渐变大。造成这一结果的原因是溶液中尿素量越多,碱性就越强,在结晶过程中,沉淀过程加快,团聚现象增加,样品粒径就逐渐变大。
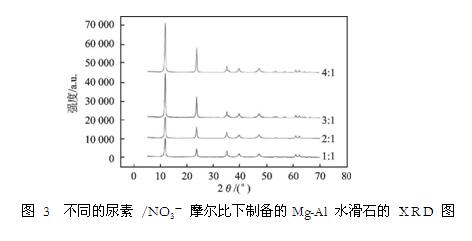
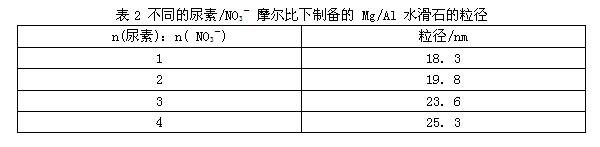
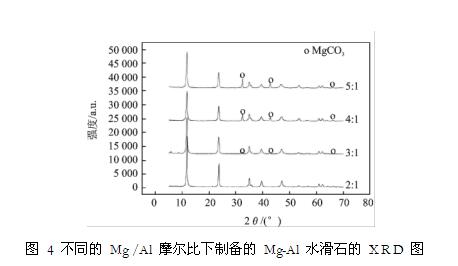
图4绘出了n(尿素):n(NO3-)= 3:1,n(Mg):n(Al) =2~5的 XRD 谱图。由图4可知,n(Mg):n(Al) =2:1时,制得的水滑石样品比较纯净;随着 n( Mg): n( Al)的增加,会有 MgCO3 的杂质峰出现。通过对样品做定量分析得出n( Mg): n( Al) = 2:1时,样品中水滑石含量可达到100%,而随着 Mg 源的增加,样品中水滑石的含量会降低到 75% ~80%。
2.3 SEM 表征
把以菱镁矿为原料制备的水滑石样品和以硝酸镁试剂为原料制备的水滑石样品进行SEM对比分析,得到图5(其中,样品a 的原料为菱镁矿,样品 b的原料为 硝酸镁试剂)。制备条件均为n(Mg):n(Al) =2∶1,n(尿素):n(NO3-) =3:1。


由图可以明显看出, a 样品层要比 b 样品层厚很多, 而且 b 样品有团聚现象, 样品的的形貌更趋于六边形。这说明天然存在的菱镁矿必然有杂质存在,制备出的硝酸镁纯度低,会影响结晶过程,制备出的样品自然要比用硝酸镁试剂制备的样品层厚。
3 结论
以菱镁矿分解的氧化镁为原料,采用尿素法制备 Mg- Al 水滑石。菱镁矿分解的最佳条件为700 ℃下煅烧 0.5 h。通过 XRD 分析得出当溶液中 n(尿素):n(NO 3-)= 3:1时,合成的水滑石样品具有较高的结晶度;当 n( Mg):n( Al) =2:1 时,合成的水滑石纯度可达到 100%; n( Mg):n( Al) 继续增大时,会有MgCO 3杂质产生;n(Mg):n(Al) =2:1,n(尿素):n( NO3-) =1~4 时,水滑石样品的粒径尺寸分别为 18.3,19.8,23.6,25.3 nm。通过 SEM 图看出菱镁矿合成的样品层要明显比硝酸镁试剂合成的样品层厚很多。
【参考文献】
[1]赵海鑫.辽宁菱镁矿资源现状及发展意见[J].耐火材料,2009,43( 4):291- 293.
[2]邸素梅.我国菱镁矿资源及市场[J].非金属矿,2001,24(1):5- 6.
[3] 王兆敏.中国菱镁矿现状与发展趋势[J].中国非金属矿工业导报,2006( 5):6- 8.
[4]张兴业.提高我国菱镁矿资源利用率的途径[J].矿产保护与利用,2008(4):23- 25.
[5]李志锋.辽宁低品位菱镁矿的综合开发利用研究[J].国土资源2008(z1) :78- 79.
[6]Cavani F,Trifiro F,Vaccari A.Hydrotalcite type anionic clays:preparation, properties and applications[J]. Catalysts Today,1991, 11(2):173- 301.
[7]Fabio Papini. Synthesis and modification of hydrotalcite as a thermal stabilizer for poly( vinylchloride)[D].Leicestershire:Loughborough University, 2010.
[8]Zou Yong,Alírío E Rodrigues. Hydrotalcite-like compounds as adsorbents for carbon dioxide[J]. Energy Conversion and Management,2002, 43(14):1865- 1876.
[9]Umberto Costantino,Valeria Ambrogi,Morena Nocchetti,et
al.Hydrotalcite-like compounds:Versatile layered hosts of molecular anions with biological activity[J].Microporous and Mesoporous Materials,2008,107(1/2):149- 160.
[10]周琳.类水滑石的制备及相关结构研究[D]. 北京:北京化工大学,2007.
[11]任志峰,何静,张春起.焙烧水滑石去除氯离子性能研究[J].精细化工,2002,19( 6):339- 342.
[12]吕亮.层状双金属( 氢) 氧化物对卤离子的吸附和离子交换性能研究[D].北京:北京化工大学,2005.
[13]邓欣,曾虹燕,冯震.纳米晶镁铝水滑石制备机理及抗毒性研究[J].功能材料, 2007,38(6):965- 967.
[14]杨飘萍.尿素法合成高结晶度类水滑石[J].无机化学学报,2003, 19(5):485- 489.
[15]张瑞峰.反应时间对镁铝水滑石制备及其性能影响[J].大化科技, 2008(1):4- 6.
上一篇:萤石特点及其应用现状
下一篇:无





