制备高纯氧化镁的工艺研究
- 发布人:管理员
- 发布时间:2012-12-05
- 浏览量:1358
王亚芳 , 仲剑初* , 王洪志
摘要:本文以轻烧镁为原料,经消化、碳化、除杂、热解及煅烧制备出高纯氧化镁,并确定了适宜的工艺条件:碳化固液比20g/L,时间60min;活性炭吸附除杂温度20℃,时间80min;热解温度100℃,时间20min,升温速率均匀缓慢;煅烧温度950℃。氧化镁产品中MgO含量可达99.5%,CaO含量小于0.09%,Fe的含量小于0.05%,产品中粒度小于5μ的粒子达到72.3%。SEM分析表明,低温热解氧化镁为针状,高温热解氧化镁为球状。
关键词:轻烧镁;高纯氧化镁;除铁;活性炭
氧化镁作为一种重要的无机化工产品,用途非常广泛,主要用于耐火材料和提炼金属镁,其次也用于纸浆、提铀、建筑材料、肥料、橡胶、塑料和粘合剂等[1-3]。
高纯氧化镁制备的方法主要有气相氧化法、液相滴入法、Sulmag法、Aman法、金属醇盐法等。菱镁矿是制取氧化镁产品的主要原料之一,储量十分丰富,轻烧镁主要是以菱镁矿为原料经在700℃~1000℃的温度下煅烧而制得[4-6]。以往国内由矿物原料生产的氧化镁纯度低于97%,使其应用受到限制,产品的附加值较低。高纯氧化镁一般指MgO≥98%的产品,由于产品纯度提高,应用领域扩大,应用于相应行业的产品如冶金、橡胶、电子等行业产品质量也相应提升[7-10]。因此高纯氧化镁开发及实现工业化,将对电子、国防、航天及高级陶瓷等行业的发展起到极大的促进作用。高纯氧化镁的制备涉及到钙、镁分离及铁等杂质的脱除,由于钙、镁的化学性质相近,用化学方法很难分离,本文选择活性炭为吸附剂脱除杂质。活性炭及其他吸附剂吸附金属离子及有机化合物在环保方面的报道较多[11-16] ,但在无机盐工业中作为除杂吸附剂的研究甚少。本文以轻烧镁为原料经消化、碳化制得碳酸氢镁溶液,采用活性炭为吸附剂脱除碳酸氢镁溶液中的铁离子,系统的研究了制备高纯氧化镁的工艺过程。
1 实验部分
1.1 试剂和仪器
1.1.1 试剂及原料
试验中所用的试剂及原料有:活性炭(AR,天津南开化工厂)、30%盐酸(AR,大连海运试剂厂)、EDTA(AR,吉林省军区化工厂)、CO2(市售)、轻烧镁(菱镁矿在750℃以下烧成,辽宁海城)等。轻烧镁主要化学组成:MgO 82%,CaO 1%,Fe2O3 0.6%,其他6.4%。活性炭使用前需经盐酸进行预处理。
1.1.2 仪器
LY-2型碳酸化反应釜、DB-101S型集热式恒温磁力搅拌器、721分光光度计、SA-CP3离心粒度仪、KYKY2800B扫描电镜。
1.2 实验方法及原理
原料轻烧镁经消化、碳酸化、过滤得到碳酸氢镁溶液,准确称取适量已处理的活性炭及活化剂加到1500mL碳酸氢镁溶液中,然后置于恒温磁力搅拌器中进行吸附脱除反应。在选定的温度下,每隔一定时间抽取悬浊液50mL转移至布氏漏斗中快速真空抽滤,用721分光光度计测定滤液中铁含量,用EDTA测定分析钙、镁组分。镁、铁吸附量Q(mg/g)按下式计算:
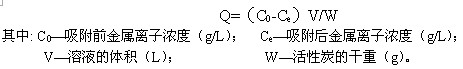
经过滤除杂后的碳酸氢镁溶液进行热解,热解的方式有两种:一种是将磁力搅拌器的水浴温度设定,然后放入碳酸氢镁溶液,逐渐升到设定的温度下进行热解;另外一种是直接明火加热,快速升到指定的温度进行热解。过滤热解液,得到的碱式碳酸镁经干燥后,在马弗炉中进行煅烧,得到的氧化镁产品进行组成分析、粒度分布的测定及晶型观察。
2 结果与讨论
2.1 轻烧镁乳液的碳化过程
2.1.1 碳化时间对浸出浓度的影响
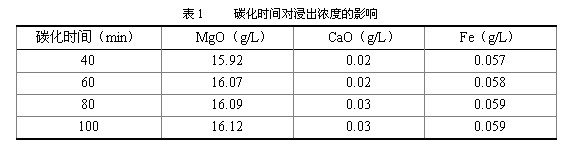
轻烧镁经消化降至室温,在压力为0.1MPa、转速为1000rpm下碳化反应,40min后开始取样,以后每隔20min再取样,分析浸出液中各组分的含量。碳化时间对各组分浸出浓度的影响见表1。由表1可见,碳化时间对浸出浓度的影响不明显,60min后各组分的浓度基本恒定。因此在以后的实验中,均选择碳化时间为60min。
2.1.2 固液比对轻烧镁中镁、铁离子浸出率的影响
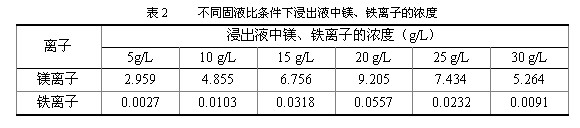
为考察固液比对轻烧镁中镁、铁的浸出率的影响,实验中选择的固液比为5g/L、10 g/L、15 g/L、20 g/L、25 g/L和30 g/L,不同固液比的消化悬浊液经碳化后得到碳酸氢镁溶液,测溶液中镁、铁离子浓度,结果见表2。由表2可见,镁、铁离子浓度随固液比增大而增大。但是,当固液比达到20 g/L时,镁、铁离子的浓度均达到最大值,此时镁的浸出率大于93%。固液比大于20 g/L以后,镁、铁离子的浓度开始下降,且浸出率急剧下降,至30 g/L时镁的浸出率只有35%左右。这一现象表明,当溶液中镁的浓度过高时,会使部分碳酸氢镁转化为碱式碳酸镁沉淀,从而使镁离子浓度下降。而铁离子浓度的降低是由于沉淀的碱式碳酸镁吸附的原因。因此,碳化反应适宜的固液比为20 g/L。
2.2 杂质脱除
2.2.1 温度和时间对吸附脱除反应的影响
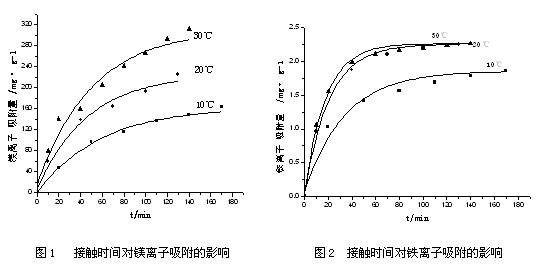
为获得高纯氧化镁,必须对碳化过滤后得到的碳酸氢镁溶液进行净化处理,除去其中Ca2+和Fe3+等杂质离子。由于Ca2+和Mg2+离子的性质相似,用普通的化学方法很难分离,本文以活性炭为吸附剂,同时脱除碳酸氢镁溶液中的钙、铁离子。为考察温度和时间对吸附反应的影响,实验中选择了三个吸附温度:10℃、20℃及30℃,时间为10min~140min。在不同的温度下,活性炭对镁、铁的吸附量随时间变化的规律如图1和图2所示。 由图1、2可知,吸附量随时间及温度的增加而增大。温度对镁的吸附影响较大,低温时吸附量较小,高温时吸附量较大。因此,从提高产品收率角度考虑,应在低温下进行吸附除杂。从图2结果可知,20℃吸附铁的效果比10℃好,达到平衡的时间快,而且吸附量大,20℃~30℃的吸附曲线相近,表明在20℃~30℃之间温度对铁吸附反应影响较小。
2.2.2 活性炭除铁工艺条件的选择
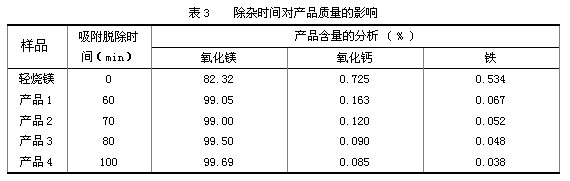
由上节有关活性炭对镁,铁吸附平衡分析可知,当吸附温度为20℃,接触反应80min,镁的吸附量适中,而铁的吸附量较大,符合产品净化原则。为了确定除铁的适宜工艺条件,以最终氧化镁产品中铁和钙的含量为目标参数进行考察。即将500ml碳酸氢镁溶液置于20℃水浴中,加入活化剂及不同量的活性炭,热解后,在950℃下煅烧2h,得到的氧化镁的含量均超过99.0%。当加入活性炭16g/L时,吸附反应120min,产品中铁的含量降至0.049%;当加入活性炭20g/L,吸附反应80min,铁的含量为0.048%;而加入活性炭60g/L时,吸附脱除60min,铁的含量就达到0.048%。考虑到活性炭的消耗量及处理时间,活性炭的用量以20 g/L为宜。在20℃及活性炭用量20g/L条件下,分别吸附反应60min、70min、80min、100min,考察吸附脱除时间对产品氧化镁质量的影响。除铁后的母液经热解获得碱式碳酸镁,碱式碳酸镁在950℃下煅烧以后,得到氧化镁并分析其组成,实验结果见表3。由表3可见,经过不同时间吸附除杂后,氧化镁产品中MgO含量均达到99%以上,但钙、铁含量却有明显差异。高纯氧化镁要求CaO含量<0.5%,Fe<0.05%。经过60min和70min吸附脱除,虽然产品中CaO指标小于0.5%,但铁含量指标不合格。而经过80min和100min吸附除杂,铁含量指标均在0.05%以下。因此采用活性炭除杂的工艺条件以20℃,活性炭用量20g/L,吸附反应80min为宜。
2.3 热分解
影响产品MgO粒子大小及粒度分布的因素较多,除碳酸氢镁溶液中MgO的含量之外,热解温度及方式等对氧化镁的粒度分布有较大影响[17]。许多高纯专用氧化镁对产品的粒径大小及粒度分布均有一定要求,因此有必要探讨氧化镁粒径分布控制的条件,采用SA-CP3离心粒度仪测定粒度分布。
2.3.1 热解产物
热解、干燥后得到的产物进行了X射线衍射分析,结果如图3所示。XRD图谱特征峰与4MgCO3·Mg(OH)2·4H2 O的特征峰一致, 表明产物是4MgCO3·Mg(OH)2·4H2 O。在热分解过程中,碳酸氢镁溶液中碳酸氢镁受热发生水解,Mg2+分别同溶液中的CO32-和OH-结合,形成4MgCO3·Mg(OH)2·4H2 O的晶种,然后长大形成微粒,微粒粒子以一定的晶型定向排列到晶核上,形成一定晶型的沉淀物。

2.3.2 热解温度和时间的影响
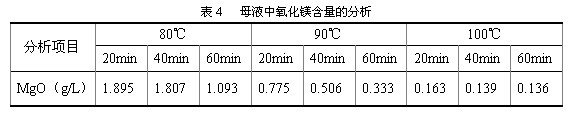
表4是热解后母液中氧化镁的含量。从表4可以看出,温度升高,母液中残留的氧化镁含量逐渐减少;在同一温度下,时间增加,母液中氧化镁的残留量也逐渐减小。在较高温度时,氧化镁浓度减小的趋势缓慢;如在100℃时,热解20min后,母液中氧化镁浓度几乎不变,说明热解基本完全。
热解时间、热解温度及升温的速率对最终的氧化镁产品晶形及粒度分布均有一定影响。在热解温度和时间分别为100℃、20min条件下,考察了升温速率对粒度分布的影响;均匀缓慢升温时,粒度小于5μ的氧化镁产品占72.3%;升温速率较快时,粒度小于5μ的产品只有51.9%。当升温速率缓慢且均匀时,在100℃下热解20min,粒度小于5μ的氧化镁产品达到72.3%;热解时间为60min,小于5μ达到72.1%。在升温速率均匀缓慢及热解时间20min的条件下,热解温度为60℃时,粒度小于5μ的产品达到92.4%,小于3μ的产品达到63.7%;而当热解温度为80℃时,小于5μ的产品占79.3%, 小于3μ的产品只有22%。为了解热解温度对最终氧化镁产品晶型的影响,对不同热解温度下得到的氧化镁粉末进行SEM分析。图4A是在60℃下热解得到的针状氧化镁晶体SEM照片,图4B为80℃热解后得到的针状氧化镁晶体SEM照片,图4C为100℃热解后得到的粒状晶体照片,图4D为直接加热,快速升温到100℃,得到大的凝聚物。
从上面实验数据可以得出下面结论:热解时间对产品氧化镁的粒度分布影响甚微。升温速率过快,最终的氧化镁产品粒径较大。热解温度不仅对氧化镁产品粒径有直接影响, 而且对氧化镁的晶形也有较大影响。热解温度高,产品的粒径随之增大。这是由于温度过高,晶粒生长速度加快,容易形成大的晶粒。升温速率过快由于受热迅速而形成的庞大晶核,碱式碳酸镁相互之间在溶液中产生无秩序的凝聚物而形成颗粒粗大的沉淀。热解温度较低时,氧化镁晶体为针状;热解温度较高时,氧化镁晶体呈粒状。
实验结果表明,碳酸氢镁溶液在100℃下热解反应20min,热解析出的碱式碳酸镁经煅烧后获得氧化镁,其中粒径小于5μ的氧化镁已达到72.3%。这一指标符合高纯硅钢氧化镁的要求:粒径小于5μ的粒子大于70%。

3 结论
碳化时间对各组分浸出浓度的影响较小,选择60min为宜。固液比对轻烧镁中镁、铁离子的浸出率影响较大,开始时随着固液比的增大,镁、铁离子浓度增大;当固液比达到20g/L时,镁和铁离子的浸出浓度达到一个最高值。适宜的固液比为20g/L。
活性炭吸附脱除杂质铁离子与温度和接触时间有关。温度高铁离子吸附脱除效果好,但同时会损失较多的镁,温度应控制在20℃为宜。
制备高纯氧化镁过程中,可采用活性炭吸附脱除杂质。其适宜工艺条件为:温度20℃,活性炭用量20g/L,吸附时间80min,在此条件下,最终得到的氧化镁产品中MgO含量可达99.5%,CaO含量小于0.09%,Fe的含量小于0.05%。
热分解对MgO粒子大小及粒度分布影响较大,这是控制氧化镁粒径的关键步骤。热解的时间对粒度的分布影响较小,温度及升温速率却有较大的影响。温度高,粒径变大,升温速率过快容易形成较大的凝聚物。控制温度为100℃,时间为20min,缓慢升温,得到颗粒细小的微晶MgO,粒度小于5μ的粒子达到72.3%,分散性好。 (作者单位:大连理工大学精细化工国家重点实验室)
下一篇:推动科技创新-促进行业健康发展





